
.
Plusieurs théories ont été élaborées relativement au développement des tumeurs :
1/ la théorie de l’irritation de Virchow et de l’hyper-régénaration de Fischer-Wasels : les irritations chroniques altèrent l’équilibre tissulaire et provoquent la métaplasie (malrégénération). Ex.: cancer de l’estomac suite à un ulcus gastrique récidivant, cancer du foie sur cirrhose, cancer du poumon sur bronchite chronique …
.
2/ la théorie de la mutation cellulaire de Borst et Bovari : l’altération de l’ADN cellulaire permet à la tumeur de se développer. Sont ainsi expliqués le rôle : des radiations ionisantes (ex.: leucémies), des carcinogènes chimiques (ex.: amiante, cadmium, chrome, goudrons …), des virus oncogènes (ex.: EBV, papilloma virus …), des parasites (bilharziose et K de la vessie), des prédispositions héréditaires (ex.: polypose intestinale).
.
3/ récemment, la mise en évidence d’une protéine du noyau (nommée « P53 ») régulant la prolifération cellulaire, a fait naître de nouveaux espoirs …
.
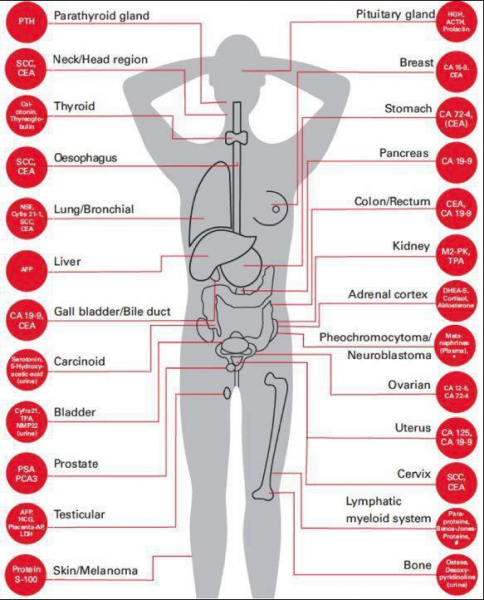
L’apparition de marqueurs biologiques assez spécifiques est d’un grand intérêt pour évaluer le potentiel évolutif, la réponse à la thérapeutique et les éventuelles récidives. Ces marqueurs tumoraux, sont des substances protéiques dont la présence dans le sérum est liée à l’existence d’une tumeur maligne, le marqueur idéal se doit d’être :
.
Certains marqueurs (imparfaits) sont bien connus :
.
La découverte récente d’un récepteur tissulaire de la FSH a fait naitre de nombreux espoirs, car cet agent de la croissance tissulaire est positif pour plus de 10 cancers différents.
Pour les médecins qui en ont la pratique, le typage lymphocytaire représente l’examen de choix pour le suivi du terrain cancéreux (cf. CAC de Villejuif). On peut y observer :
.
Un cancer peut apparaître dans n’importe quel tissu ou organe et à tout âge, leur cause reste inconnue dans 85 % des cas. La majorité des cancers détectés à un stade précoce sont à présent potentiellement curables, les organes ectodermiques ou encapsulés ont des pronostics plus favorables. Le pronostic conditionne le choix thérapeutique, car un fort degré de dédifférenciation, un envahissement ganglionnaire ou une métastase sont de mauvais pronostic (10% des cancers sont révélés par une métastase !). Le système de cotation TNM prend en compte :
Ainsi, un cancer du sein classé « T3N2MO » signifie que la tumeur est supérieure à 5 cm, qu’il existe une adénopathie axillaire palpable et fixée et que l’examen clinique ne permet pas de déceler de métastase à distance. On complète ce code anatomique d’une appréciation de la dé-différentiation tissulaire :
On peut aussi préciser la vitesse de l’envahissement tumoral en calculant l’index mitotique (% de cellules cancéreuses en phase de mitose, ou (plus précis) leur « temps de doublement potentiel », indice intéressant pour quantifier la prolifération tumorale et mieux adapter le traitement, en particulier la radiothérapie.
.
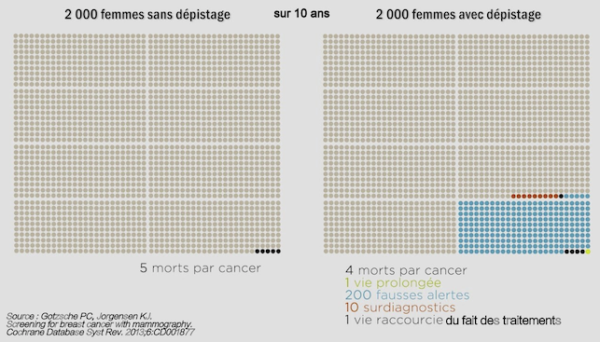
C’est ce qui a poussé l’état à généraliser la mammographie, dans le but de favoriser le dépistage précoce des cancers du sein. Or, la méthode s’est avérée contre-productive et le dépistage systématique devrait prochainement être abandonné :
.
.
Il dépendra du stade de la maladie, différentes combinaisons étant possibles : chirurgie (qui passera en tissu sain avec évidemment ganglionnaire si nécessaire) et/ou radiothérapie (lorsque la tumeur est localisée), chimiothérapie, hormonothérapie (qui supprime l’activation hormonale qui entretient la prolifération) et/ou immunothérapie (lorsque l’extension ne permet plus l’exclusion tumorale). Ces interventions sont guidées par les progrès des méthodes de localisation tumorale : échographie, fibroscopie, scintigraphie isotopique, scanner et IRM.
.
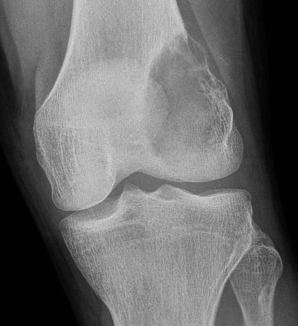 Métastase osseuse d’un cancer du rein
Métastase osseuse d’un cancer du rein
.
La radiothérapie est utile lorsqu’un foyer est localisé (peau, séminome, prostate) ou dans les lymphomes (Hodgkin, LLA) ou à titre palliatif : métastases osseuses (réduit les douleurs et le risque fracturaire) ou cérébrales. Elle utilise à présent des rayonnements de haute énergie (des rayons gamma jusqu’au particules lourdes), la technique des « feux croisés » et du calcul par ordinateur des isodoses délivrées aux tissus profonds.
.
La « radiochirurgie » (Gammaknife) est par exemple une technique qui par stéréotaxie traitera les lésions intra-craniennes. L’unité utilisée est le Gray (= 100 rads ou 100 Kjoules/kg). Un traitement délivrera de 3 à 60 Grays en 4 à 6 semaines (n.b. irradiation naturelle = 4 milliGrays/an). Une nouveauté semble avoir beaucoup de succès dans plusieurs centres : la radiothérapie per-opératoire … Les aplasies médullaires, les nécroses ou les fibroses douloureuses ainsi que les lymphoedèmes, en constituent des complications classiques.
.
La « curiethérapie » est une variante utilisée sur les organes difficilement accessibles (base de langue, col utérin, rectum …). Elle utilise des fils d’Iridium 192 (période 72 jours).
.
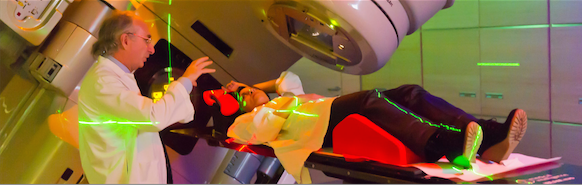 radiothérapie ciblée
radiothérapie ciblée
.
La chimiothérapie est en progrès (surtout par l’utilisation séquentielle de plusieurs agents cytotoxiques, selon les phases des mitoses cellulaires, lors du doublement de la quantité d’ADN). Exemples de produits classiquement utilisés selon la cinétique cellulaire =
« G0 » phase de repos (surtout les cellules normales)
« G1 » phase précédant la synthèse de l’ADN (12 heures à quelques jours) … l’ADN se déroule
« S » phase de synthèse de l’ADN (2 à 4 heures) : on délivre alors les antimétabolites
« G2 » phase tétraploïde (2 à 4 heures) : on délivre alors les antibiotiques intercalants : Streptomyces (Bléomycine)
« M » mitose : les antimitotiques … Alcaloïdes végétaux : Vinca major (Vinblastine, Vinorelbine), Podophyllotoxine, Taxus baccata (Taxol), Etoposide (Mandragore) et Colchicine.
.
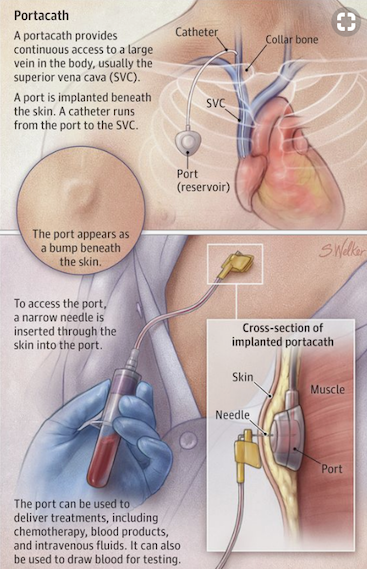 Chambre implantée
Chambre implantée
.
Cinq classes de produits sont utilisées :
Certains remèdes (Cis-platine, interférons, hormones) ne présentent pas de spécificité de phase.
.
La chimiothérapie utilise aussi parfois des pro-drogues : molécules activées par un enzyme dans l’organisme (ex.: la Leurimicine, le Carbo-platine) … ou la « photo-chimiothérapie », c’est à dire l’illumination locale (bouche / œsophage / peau…) de petites tumeurs préalablement marquées par une substance photo-sensibilisante (dérivée de l’hématoporphyrine).
.
De nouveaux produits sont toujours essayés, comme actuellement le « Votrient » dont le principe actif toxique est le pazopanib (inhibiteur des protéines impliquées dans la croissance et la dissémination des cellules néoplasiques).
.
.
NB. Les traitements radio et chimiothérapiques puissants ont des limites naturelles : la neutropénie fébrile, la thrombopénie, des mucites ou diarrhées, des complications hépato-rénales, parfois même des leuco-encéphalites ! De plus, ces traitements sont tératogènes. Le problème se complique quand la phase immunodépression (agranulocytose et risque de reprise tumorale rapide) se complique d’une surinfection ou de la réactivation d’une virose chronique (ex.: CMV). Les aplasies médullaires peuvent être limitées par l’utilisation de facteurs de croissance comme le G-CSF ou GM-CSF.
.
La limite des méthodes classiques est admise dès 1974 par le Pr. Mathé : « Lorsqu’un patient est en phase perceptible de la maladie, il porte en lui environ un kilogramme de cellules tumorales (soit 10 puissance 12). Une rémission apparemment complète peut être obtenue par une chimiothérapie. Mais le patient est encore porteur d’une maladie résiduelle qui peut se limiter à un gramme de cellules (soit 10 puissance 9) disséminées dans l’organisme« . C’est sur ce reliquat cellulaire que vont s’exercer l’hormonothérapie et l’immunothérapie (classique ou non), ce qui fera la différence entre guérison et récidive !
.
Autre revers des chimiothérapies « modernes »: nous observons de plus en plus de rechutes tumorales précoces. En effet, le tissu lymphoïde ayant supporté des doses plus fortes, l’immuno-dépression induite ouvre la porte aux récidives ! Le dr Ph. Lagarde, confrère cancérologue niçois, a fait parler de lui ces dernières années, en prônant des formules originales de micro-chimiothérapie continue, en lieu et place des doses brèves et puissantes, classiquement utilisées … après des années de procédures diverses (dont trois semaines de prison, alors qu’il était acquitté quelques années après !), celui-ci a du jeter l’éponge en France et dirige actuellement une des plus grandes centre anticancéreux privées d’Europe, en Italie !
.
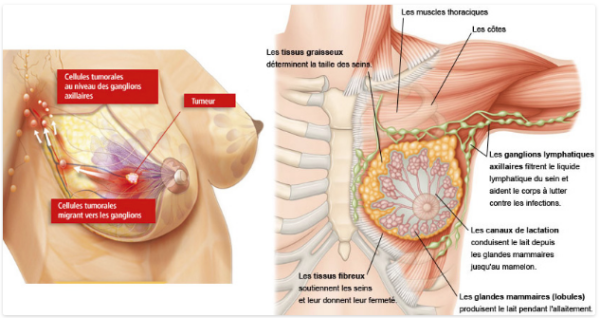
Les cancers hormono-dépendants (ex. 2/3 des cancers du sein peuvent bénéficier d’un traitement ciblant ces récepteurs oestrogéniques). On utilise ainsi, selon des protocoles variables (voir chapitre spécifique) :
.
Exemple de traitement chimiothérapique pour un myélome : 12 semaines, pour subir ensuite une autogreffe et séjour en chambre stérile.
.
Adjuvants utilisés à présent :
1/ Différentes formes d’immunothérapie ont été essayé, avec des succès certains (voir chapitre spécifique)
.
2/ Les rétinoïdes (proches de la vitamine A) qui favorisent la différentiation cellulaire représentent une voie de traitement prometteuse des cancers de la peau et des leucémies aiguës pro-myélocytaires (au prix de quelques effets secondaires).
.
3/ les agents limitant la prolifération vasculaire (néovascularisation péri-tumorale), type Avasta, se sont montrés efficaces dans certaines tumeurs (ex.: rein) et leurs métastases. Un équivalent naturel, extrait du cartilage de requin, a également donné des résultats intéressants.
.
4/ Le Dichloracétate (DCA), molécule non toxique qui agit sur la mitochondrie et limite donc la croissance du tissu tumoral (qui fonctionne par transformation du glucose en pyruvate, puis en acide lactique). Des essais sont en cours dans les glioblastomes (tumeurs cérébrales très agressives), avec des résultats encourageants (Michelakis et coll. dans « Science Translational Medicine« , 12 mai 2010).
.
5/ A noter le rôle adjuvant des biphosphonates (Clastoban) administrés en IV ou per os, qui inhibent la fonction ostéoclastique et réduisent donc le risque de fracture des métastases osseuses, surtout des cancers du sein et des myélomes, comme des hypercalcémies malignes.
.
6/ ZARZIO 30 (Filgrastim, facteur méthionylé recombinant humain stimulant des colonies de granulocytes (G-CSF), produit dans E. coli par la technique de l’ADN recombinant.
.
Problème souvent mis en avant par les centres anti-cancéreux : les plantes ont des effets protecteurs hépatiques et donc réduisent ou modifient l’effet des chimiothérapies :
.

.
Notre but est de mettre à disposition des internautes (étudiants, professionnels de la santé et patients) les renseignements disponibles dans le domaine des médecines douces (en anglais, l’on parle de « complementary and alternative medicine »), au sein d’un concept global d’équilibre du terrain, pour qu’ils participent avec nous au débat ouvert sur la médecine de demain … dans une approche systémique de la santé, des symptômes et des remèdes !
Vous appréciez les articles de notre site ?
Vous vous intéressez à la santé naturelle et à la médecine fonctionnelle ?
Laissez nous votre email pour recevoir toutes les semaines des articles, des infos et des conseils