
.

.

.
L’immunologie progresse, tant sur le plan théorique (expliquant la pathogénie de nombreuses maladies, comme les thyroïdites, le diabète insulino-dépendant ou la myasthénie) que thérapeutique (avec l’apparition des AC monoclonaux), prenant une part croissante en médecine : Les maladies auto-immunes touchent à présent 7 % des européens. Leur fréquence, leur chronicité, la gravité des lésions qu’elles entraînent, leur résistance fréquente aux médicaments font de ces affections un véritable fléau.
.
Leur pathogénie est considérée comme mystérieuse. On constate que l’individu développe une réponse immunitaire aberrante dirigée contre certaines de ses propres structures. Quelquefois, on connaît certains rouages du processus pathologique, par exemple le rôle des anticorps antirécepteurs de l’acétylcholine dans la myasthénie ou le rôle des lymphocytes T4 dans le diabète sucré juvénile.
.
.
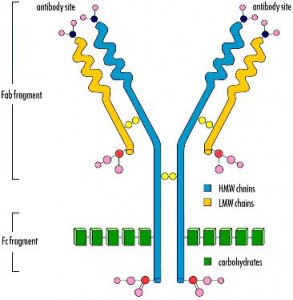
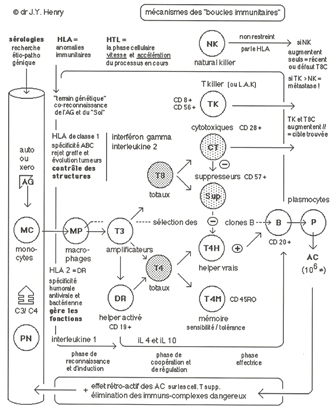
La réponse immunitaire normale est un phénomène complexe :
Considérons des cellules porteuses d’antigènes, venues de l’extérieur et ayant pénétré dans un organisme humain, par exemple des leucocytes apportés par une transfusion sanguine. Les macrophages de l’hôte phagocytent ces cellules et en extraient une information antigénique qu’ils transmettent aux lymphocytes T4 auxiliaires. Les T4 vont recruter des T8 cytotoxiques et des lymphocytes B . Les T8 vont reconnaître les antigènes sur les cellules cibles et exercer une action lytique sur les leucocytes étrangers. Les B se différencient en plasmocytes qui produisent des anticorps spécifiques des antigènes des cellules cibles. Les anticorps vont s’accrocher à des macrophages et des polynucléaires neutrophiles qui phagocytent les cellules étrangères. S’accroche aussi à ces AC la chaîne des facteurs du complément qui exerce un effet lytique. Enfin, les T4 suscitent également l’activation de T8 suppresseurs qui arrêtera la réponse immunitaire, lorsqu’elle a rempli son but, et la formation de T4 mémoire qui conservent le souvenir de l’antigène. De nombreuses cytokines interviennent aux différents stades.
.
.
Chez l’individu normal, la tolérance pour les auto-antigènes n’est pas absolue : 10 à 30 % des Lymphocytes B (CD45) fabriquent des auto-anticorps. La plupart de ces auto-anticorps sont des IgM polyspécifiques inoffensifs. Cette auto-immunité est physiologique, à la base d’un effet cytotrophique (de rajeunissement tissulaire, par éliminations des cellules lésées ou vieillissantes) donc protecteur, contrairement aux maladies auto-immunes qui sont caractérisées par une réponse immunitaire cellulaire et/ou humorale agressive, susceptible de provoquer des lésions ou des anomalies de fonctionnement de certains organes. Quand des auto anticorps sont présents dans les maladies auto-immunes, il s’agit d’IgG, ayant une spécificité précise et une forte affinité pour les auto-antigènes. Pour affirmer le caractère auto-immun, il faut avoir identifié l’auto antigène et l’auto-anticorps. Ces critères semblent trop restrictifs, car ils manquent dans de nombreux états pathologiques pourtant étiquetés « auto-immuns ».
.
.
Les maladies auto-immunes sont polyfactorielles. Leur développement nécessite la conjonction de facteurs génétiques et de facteurs environnementaux. Pour comprendre le mécanisme de l’auto-immunité pathologique, il faut identifier quels sont ces facteurs génétiques et quels sont ces facteurs environnementaux.
1er facteur lié au HLA …
La région HLA est située sur le bras court du chromosome 6, elle correspond à environ 1/1000 du génome humain. Parmi les nombreux locus appartenant à cette région, six seulement nous intéressent :
Le site de présentation des macrophages est de trop faible dimension pour reconnaître directement une bactérie, un virus ou même une protéine. Il ne peut se lier qu’à des peptides. De plus, la reconnaissance est impossible si le peptide est isolé. Il est nécessaire qu’il soit présenté au SPM par une molécule HLA. Ce phénomène, mis en évidence par BABBITT et coll. (1985), SETTE et coll. (1987) a été appelé « reconnaissance en association ». La fonction des molécules HLA (glycoprotéines), est donc de se lier à des peptides. A cet effet, chaque molécule HLA peut héberger un peptide et un seul à la fois.
2ème facteur lié aux peptides …

.
On ne trouve des peptides que dans les êtres vivants. Puisque nous avons écarté les peptides du patient, les suspects se rangent en plusieurs catégories : parasites, mycoplasmes, virus, bactéries, produits chimiques (médicaments ou implants), vaccins et aliments (ceux-ci proviennent des animaux et des végétaux qui sont des êtres vivants). Les parasites sont à exclure, car aucune relation n’a été démontrée avec les MAI. Les mycoplasmes peuvent provoquer certains rhumatismes inflammatoires dans quelques modèles animaux, mais en sont incapables chez l’homme. Quant aux virus, ils sont souvent accusés, mais sans preuve formelle. Si un virus était responsable d’une pathologie auto-immune, on devrait détecter chez tous les malades, ou au moins chez la plupart d’entre eux, des anticorps contre ce virus, de l’ADN ou de l’ARN viral. Or, à part quelques exceptions (HVB et HVC dans la cirrhose hépatique, Rougeole dans la RCH), il n’en est rien. Par élimination, il ne nous reste plus que certains produits chimiques (médicaments ou prothèses), des vaccins, les bactéries et les aliments. On connaît des affections auto-immunes provoquées par des prothèses (silicone et PR), des vaccins (hépatite B et SEP), des médicaments : Bêta-bloquants, Aldomet, L-Dopa, D-Penicillamine … provoquées par des bactéries, comme le RAA (certains streptocoques) et la spondylarthrite ankylosante (Klebsiella pneumoniae)…provoquées par des aliments, comme la maladie cœliaque et la dermatite herpétiforme (certaines céréales : blé, orge, seigle).
.
Pour pénétrer dans l’organisme humain, les peptides exogènes doivent traverser, soit la peau, soit une muqueuse. Or la peau et la plupart des muqueuses sont trop épaisses, trop étanches. Les deux seules muqueuses fragiles, parce qu’elles sont immenses et très minces, sont les alvéoles pulmonaires et l’intestin grêle. Dans les alvéoles pulmonaires ne pénètrent que peu de bactéries ou d’allergènes peptidiques (ex.: la « maladie du poumon de fermier »). Par contre, l’intestin grêle contient une flore abondante et variée, avec environ 500 espèces de bactéries, et les aliments en cours de digestion. Cependant, malgré son immensité (600 mètres carrés) et sa minceur (1/40 de millimètre), la muqueuse normale ne laisse passer que de petites molécules et très peu de grosses molécules. La traversée de peptides de 9 à 17 acides aminés en quantité suffisante ne peut avoir lieu que si l’intestin grêle est devenu trop perméable.
.
Le pr. Jean SEIGNALET (Faculté de Médecine de Montpellier) attribuait la responsabilité des MAI essentiellement à des peptides bactériens et alimentaires. Quelques travaux publiés sont en faveur de cette hypothèse :
* Dans la spondylarthrite ankylosante, VEYS et MIELANTS (1993) ont observé des lésions intestinales inflammatoires avec hyper perméabilité chez 209 patients sur 354 explorés. WENDLING (1992) a indiqué que ces perturbations sont présentes avant l’administration d’anti-inflammatoires.
* Dans la polyarthrite rhumatoïde, FAGIOLO et coll. (1989) ont rapporté une hyper perméabilité du grêle, alors que GENDRE et coll. (1982), O’FARRELLY et coll. (1988) constataient une atrophie des villosités chez environ 50 % des patients.
.
3ème facteur lié aux hormones …
.
Il est frappant de constater que la majorité des MAI, celles qui sont associées à HLA-DR ont une nette prédominance féminine. Ainsi la proportion des femmes par rapport aux hommes est de :
- 4 contre 1 dans la polyarthrite rhumatoïde
- 8 contre 1 dans le syndrome de Gougerot-Sjögren,
- 10 contre 1 dans le lupus érythémateux disséminé.
- 1 pour 3 dans la spondylarthrite ankylosante (HLA-B)
Ceci suggère l’intervention de facteurs hormonaux. Cette désadaptation hormonale est d’ailleurs caractéristique des phase 4, 5 et 6 de Reckeweg.
Ils agissent vraisemblablement en favorisant ou en défavorisant l’expression aberrante des molécules HLA-DR sur les cellules cibles de la réponse auto-immune.
.
4ème facteur lié au stress psychologique …
.
Dans les MAI associées à HLA-DR, on retrouve très souvent un stress qui a précédé de peu l’épisode initial et les poussées ultérieures. Un interrogatoire attentif découvre ce stress au moins 80 fois sur 100 dans la polyarthrite rhumatoïde et 90 fois sur 100 dans la maladie de Basedow ( ROSCH 1993 ). L’agression qui a entraîné le stress est très variable : maladie ou décès d’un être cher, mésentente familiale, pressions subies dans l’exercice professionnel, échec sentimental, infection bactérienne ou virale, dépense physique ou intellectuelle excessive, etc… On rencontre aussi bien des agressions brutales que de petites agressions chroniques. L’effet immunitaire des stress s’explique par les communications multiples qui relient le système nerveux central et la réponse immunitaire (REICHLIN 1993 et BLALOCK 1994). Lorsqu’ils subissent une agression, les neurones libèrent des neuropeptides dont beaucoup peuvent se fixer sur des récepteurs portés par les lymphocytes et les macrophages. Ce processus provoque la sécrétion de diverses cytokines, en particulier l’interféron g , fabriqué principalement par les lymphocytes Th1 qui favorise le développement de la réaction auto-immune.
.
.
La présence de micro-irritations chroniques (« foyer perturbateur » de la neuralthérapie) d’origine dentaire (50% des cas), sinusiennes, gynécologique ou cicatricielle, va faire remonter une information nociceptive et induire des phénomènes inflammatoires chroniques (souvent à distance du foyer). Une MAI mal controlée devra donc bénéficier d’un bilan de ces éventuels foyers (panoramique dentaire indispensable) qui créent une sorte d' »auto-allumage » des phénomènes immuns.
.
.
Conclusions :
Pour Jean SEIGNALET : « Le danger vient toujours de l’intestin grêle ». C’est de lui que proviennent les peptides non soi et les protéines super antigènes. Si l’on veut s’attaquer à la cause de la pathologie auto-immune, il faut normaliser l’intestin grêle, aussi bien pour son contenu que pour sa paroi. Seuls deux autres auteurs, à notre connaissance, ont essayé la diététique comme traitement des auto-immunités : KOUSMINE ( 1983 ) et SWANK ( 1991 ) qui sont partisans d’une forte restriction des graisses animales au profit des huiles végétales, dans le cadre d’un régime alimentaire ambitieux.
.
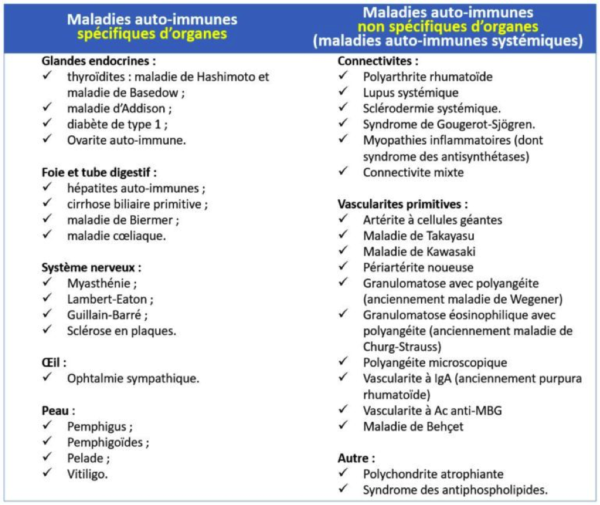
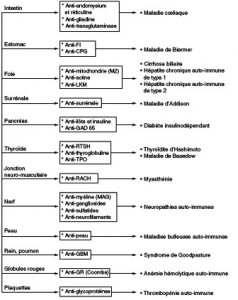
On distingue des maladies auto-immunes :
—> spécifiques d’organe (mais que l’on peut trouver associées chez un même malade), ainsi SADOVNICK et coll. (1989) ont observé une fréquence accrue du Crohn et la Recto-colite hémorragique dans la Sclérose en plaques, le Diabète sucré juvénile, le Lupus érythémateux disséminé et la Polyarthrite rhumatoïde.
—> non-spécifiques d’organes (= touchant plusieurs organes) dont le mécanisme dépend d’AC anti-nucléaires.
Outils et stratégie …
Comme vous l’avez compris, nous allons essayer d’apprécier dans chaque cas le rôle des 5 grands facteurs déclenchant des MAI.
.
L’aide d’un BNS se révèlera indispensable pour l’appréciation du stade évolutif et le choix d’un traitement physiologique, en sachant que le paramètre « Albumines » s’effondre avant et pendant les poussées de MAI, signant le passage dans une des trois « phases tissulaires ».
.
L’expérience a prouvé, BNS à l’appui, que l’utilisation d’un remède unique, comme l’isothérapie séquentielle (par exemple nosode de la typhoide) qui prétend effacer le traumatisme initial), étaient illusoires à ce stade, car les perturbations sont multiples et complexes. C’est pourquoi nous restons fidèles au principe thérapeutique de l’homéopathie diathésique : un remède en haute dilution (en fonction des symptômes) + un remède complémentaire en basse dilution (quotidiennement, pour nourrit les structures souffrantes). Si vous souhaitez réaliser un BNS12 ou 24, cliquez sur ce lien : www.mybiobox.com
.
1 / l’évaluation du HLA … bilan cher, essentiellement hospitalier (sauf HLA B 27), indiqué dès lors qu’il existe un second cas de MAI dans la famille, ou chez le même patient (vu jusqu’à trois MAI ensemble !). Plus simplement l’étude des MAI dans la lignée familiale nous renseignera de cette fragilité héréditaire.
2 / les peptides :
* microbiens … Souvent oubliés, les nosodes et stock-nosodes vont avoir un rôle déclencheur. surtout dans leur forme vaccinale (ex. typhoïde – sorte de maladie de Crohn aiguë !). L’utilisation des nosodes se justifient d’autant plus qu’il s’agit d’une « maladie grave, chronique et que rien ne soulage ». On proposera un nosode (ou Stock-nosode) unique correspondant au cas clinique (situation de « vide » de Yang, Qi, Feu, Eau, ou blocage lymphoïde ?), en haute dilution, en début de traitement si possible, mais surtout hors d’une phase aigu (sous peine d’aggravation) !
.
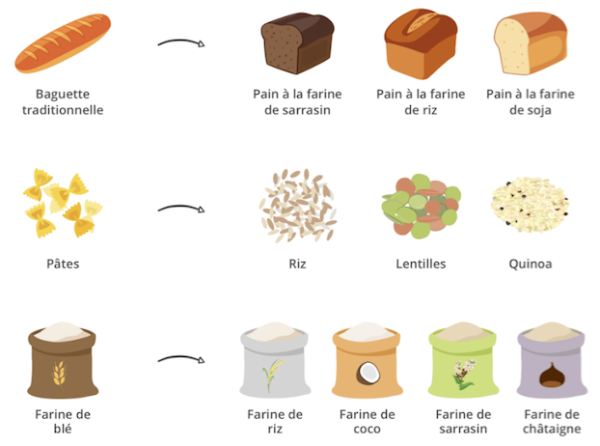
* alimentaires … problème capital pour le pr. Seignalet : régime sans gluten – blé/avoine/seigle/orge – et sans lait : efficace dans 50% des cas !
.
3 / l’équilibre hormonal … les remèdes des troubles de la sensibilité hormonale ont ici toute leur place, exemples : Pulsatilla, Sepia, Lachesis, Iodum, Thuya occ. ou Natrum sulfuricum … selon le cas.
.
4 / les « stress » psychologiques … Le sens des évènements traumatisants antérieurs est qualifié en fonction de ce que le sujet croit aujourd’hui et de sa capacité de résilience (adaptation aux malheurs). La mémoire reconstruit le passé sous l’influence des croyances présentes. On ne peut nier que les événements extérieurs ou un déterminisme biologique ont une influence sur la construction de l’individu, mais on ne peut anticiper ce qu’elle sera. D’où l’intérêt d’apprécier objectivement avec le patient son « histoire de vie » et son dynamisme psychique (capacités actuelles et existence d’un projet). Les remèdes homéopathiques seront alors une aide efficace :
.
5/ un traitement à la procaine, au laser ou par les champs magnétiques pulsés permet la plupart du temps d’éteindre le foyer perturbateur.
.
« Manuel Merck de diagnostic et thérapeutique » Edition SIDEM (MSD, USA)
« L’alimentation ou la 3 ème médecine » Jean SEIGNALET (collection écologie humaine 1996)
« La diversité des réponses immunitaires » J.F. BACH (INSERM, unité 25)
« Immuno-pathologie clinique » L.F. PERRIN et P.E. LAURENT (ed. Masson)
« Matière médicale thérapeutique » Paul KOLLITSCH (1955, réedition Hélios 1989)
.
Notre but est de mettre à disposition des internautes (étudiants, professionnels de la santé et patients) les renseignements disponibles dans le domaine des médecines douces (en anglais, l’on parle de « complementary and alternative medicine »), au sein d’un concept global d’équilibre du terrain, pour qu’ils participent avec nous au débat ouvert sur la médecine de demain … dans une approche systémique de la santé, des symptômes et des remèdes !
Vous appréciez les articles de notre site ?
Vous vous intéressez à la santé naturelle et à la médecine fonctionnelle ?
Laissez nous votre email pour recevoir toutes les semaines des articles, des infos et des conseils